Règle de remplissage : 
Pour z ≤ 20, on retiendra que les électrons remplissent les couches selon l’ordre suivant :
1s ⟶ 2s ⟶ 2p ⟶ 3s ⟶ 3p ⟶ 4s
Exemple :
Déterminer la structure électronique de chaque atome et souligner les électrons de valence.
Carbone \({}_6\text{C}\) : \(1s^2 \, \underline{2s^2 \, 2p^2}\)
Hydrogène \({}_1\text{H}\) : \(\underline{1s^1}\)
Magnésium \({}_{12}\text{Mg}\) : \(1s^2 \, 2s^2 \, 2p^6 \, \underline{3s^2}\)
Phosphore \({}_{15}\text{P}\) : \(1s^2 \, 2s^2 \, 2p^6 \, \underline{3s^2 \, 3p^3}\)
Chlore \({}_{17}\text{Cℓ}\) : \(1s^2 \, 2s^2 \, 2p^6 \, \underline{3s^2 \, 3p^5}\)
Calcium \({}_{20}\text{Ca}\) : \(1s^2 \, 2s^2 \, 2p^6 \, \underline{3s^2 \, 3p^6 \, 4s^2}\)
Les atomes tendent à obtenir une configuration électronique du gaz noble le plus proche. Pour cela ils peuvent :
Le schéma de Lewis est une représentation d’une entité chimique avec ses électrons de valence.
Exercice
| atome | Z | structure électronique | nombre d’électrons célibataires | nombre de doublets non-liants | formule de Lewis |
| H | 1 | 1s1 | 1 | 0 | |
| C | 6 | 1s2 2s2 2p2 | 4 | 0 | |
| O | 8 | [He]2s2 2p4 | 2 | 2 | |
| N | 7 | [He]2s2 2p3 | 3 | 1 | |
| F | 9 | [He]2s2 2p5 | 1 | 3 |
Exercice
| atome | Z | nombre d’électrons | structure électronique | nombre d’électrons célibataires | nombre de doublets non-liants | formule de Lewis |
| O2− | 8 | 10 | 1s2 2s2 2p6 = [Ne] | 0 | 0 | |
| Cℓ− | 17 | 18 | 1s2 2s2 2p6 3s2 3p6 = [Ar] | 0 | 0 | |
| K+ | 19 | 18 | 1s2 2s2 2p6 3s2 3p6 = [Ar] | 0 | 0 |
remarques :
3️⃣ Schéma de Lewis de molécules
| H2 | |
| HCℓ | |
| H2O | |
| NH3 | |
| CH4 | |
| O2 | |
| N2 | |
| CO2 |
limite de la théorie VSEPR : il existe des molécules stables alors que leurs structure électronique n’est pas celle du gaz noble le plus proche.
Une couche électronique est à moitié remplie.
Une lacune électronique est un déficit de deux électrons par rapport aux règles de stabilité. On la représente par une case vide dans le schéma de Lewis. Elle concerne les éléments de la colonne 2 (Be, Mg) et 13 (B et Aℓ), ainsi que les ions H+.
Exemple : le borane
Structure de Lewis des atomes Be et Cℓ :
Structure de Lewis du Chlorure de Berylium :
On remarque que :
La théorie VSEPR (valence shell electron pair repulsion) est un modèle permettant de prédire la géométrie de la molécule.
Ronald Gillespie, Londres 1958
TP − Géométrie des molécules
animation géométrie des molécules
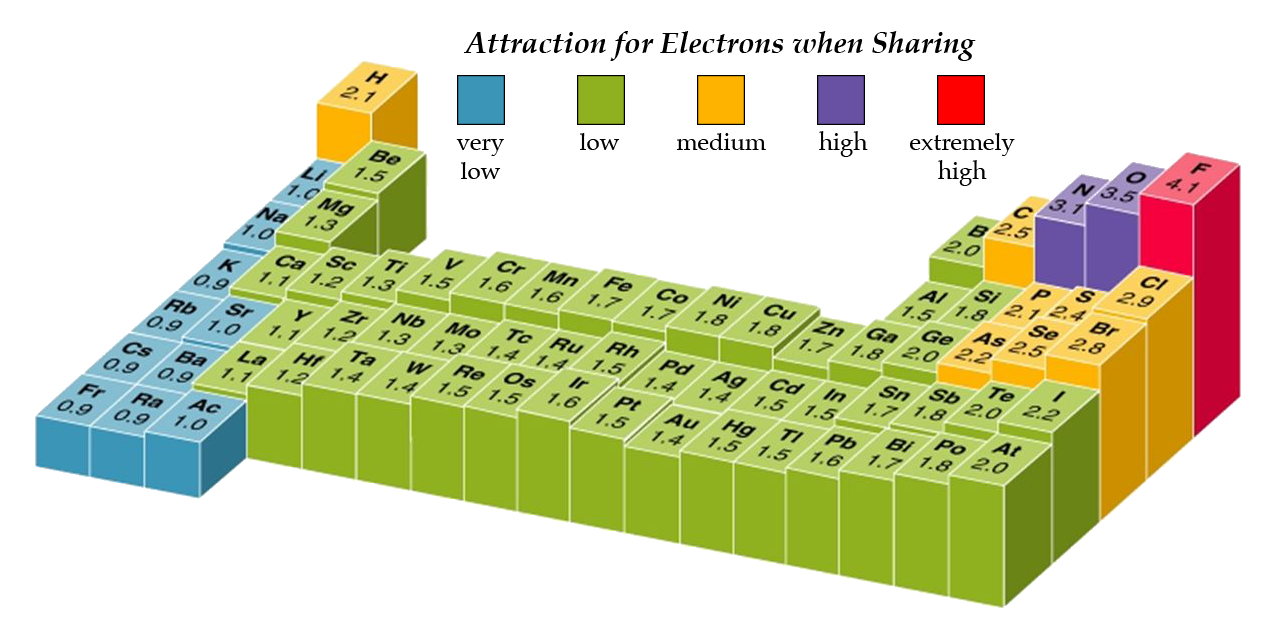
L’électronégativité d’un atome se note χ (chi). Elle traduit la capacité d’un atome à attirer les doublets d’électrons d’une liaison dans laquelle il est engagé.
L’électronégativité augmente généralement lorsqu’on va de gauche à droite et de bas en haut dans la classification périodique.
L’élément le plus électronégatif est le fluor.
La liaison est dite polaire quand la différence d’électronégativité entre deux atomes d’une même liaison est supérieure à 0,4. Les atomes portent alors une charge partielle noté δ±.
Une molécule est polaire si les barycentres des charges positives et négatives ( G+ et G−) ne sont pas confondues. Sinon elle est apolaire.
Exemples
| H2O est polaire | CO2 est apolaire |
|
|
|